
Predstavenie výrobku
| Fluorid hlinitý Základné informácie |
| Popis Syntéza Aplikácia Toxikologické štúdie Bezpečnosť Referencie |
| Názov produktu: | Fluorid hlinitý |
| Synonymá: | fluoridhlinita;TRIFLUORID HLINÍKOVÝ;FLUORID HLUNÍNÝ;Fluorid hlinitý;Fluorid hlinitý;Fluorid hlinitý;Fluorid hlinitý, 99.9+%,čistý;FLUORIDHLUNÍNÝ H |
| CAS: | 7784-18-1 |
| MF: | AlF3 |
| MW: | 83.98 |
| EINECS: | 232-051-1 |
| Kategórie produktov: | halogenid kovov; Anorganika; Anorganické fluoridy; Hliníkové soli; Hliník Veda o kovoch a keramike; Anorganika kryštalickej kvality; Veda o kovoch a keramike; Soli |
| Súbor Mol: | 7784-18-1.mol |
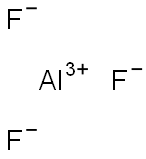 |
|
| Fluorid hlinitý Chemické vlastnosti |
| Teplota topenia | 1290 stupňov (lit.) |
| Bod varu | 1291 stupňov |
| hustota | 3,1 g/ml pri 25 stupňoch (lit.) |
| Fp | 1250 stupňov |
| rozpustnosť | Mierne rozpustný v kyselinách a zásadách. Nerozpustný v acetóne. |
| formulár | prášok |
| farba | Biela až svetlošedá |
| Špecifická gravitácia | 2.882 |
| Rozpustnosť vo vode | MIERU ROZPUSTNÝ |
| Citlivý | Hygroskopický |
| Sublimácia | 1250 ºC |
| Merck | 14,339 |
| Expozičné limity | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2 mg/m3; TWA 2,5 mg/m3 |
| Dielektrická konštanta | 2.2 (okolie) |
| Odkaz na databázu CAS | 7784-18-1(Referencia databázy CAS) |
| NIST Chemistry Reference | Fluorid hlinitý (7784-18-1) |
| Systém registra látok EPA | Fluorid hlinitý (7784-18-1) |
| Bezpečnostné informácie |
| Kódy nebezpečnosti | Xn, T, Xi |
| Výkazy o riziku | 22-36/37/38 |
| Bezpečnostné vyhlásenia | 26-37/39 |
| RIDADR | 3260 |
| WGK Nemecko | 1 |
| RTECS | BD0725000 |
| Poznámka k nebezpečenstvu | Vysoko toxický/dráždivý |
| TSCA | áno |
| HazardClass | 8 |
| PackingGroup | III |
| Kód HS | 28261210 |
| Údaje o nebezpečných látkach | 7784-18-1(Údaje o nebezpečných látkach) |
| Informácie o karte bezpečnostných údajov |
| Poskytovateľ | Jazyk |
|---|---|
| Fluorid hlinitý | angličtina |
| SigmaAldrich | angličtina |
| ACROS | angličtina |
| ALFA | angličtina |
| Použitie a syntéza fluoridu hlinitého |
| Popis | Fluorid hlinitý je vo forme bielej kryštalickej pevnej látky alebo bieleho prášku. Prirodzene sa vyskytuje ako minerály rosenbergit a oskarssonit.1 Dá sa pripraviť aj synteticky. |
| Syntéza | Fluorid hlinitý sa vyrába nasledujúcimi spôsobmi: 1) Kyselina fluorokremičitá s hydroxidom hlinitým2 H2SiF6 + 2 Al(OH)3 → 2 AlF3 + SiO2 + 4 H2O (I) Reakcia je exotermická a prebieha v niekoľkých krokoch. Dá sa opísať nasledujúcimi tromi reakciami: 3H2SiF6 + 2 Al(OH)3 → Al2(SiF6)3 + 6 H2O (II) Al2(SiF6)3 + 6 H2O → 2 AlF3 + 3 SiO2 + 12 HF (III) 12 HF + 4 Al(OH)3 → 4 AlF3 + 12 H2O Reakcia sa uskutočňuje medzi 70 °C a 100 °C. Koncentrácia kyseliny fluorokremičitej môže byť až 35 % hmotn. vo vodnom roztoku. Keďže vyrobený roztok fluoridu hlinitého je metastabilný a trihydrát začína rýchlo kryštalizovať pri teplote okolo 90°C, vyzrážaný tuhý oxid kremičitý treba čo najrýchlejšie odstrániť. 2) Al2O3 s vodnou kyselinou fluorovodíkovou3 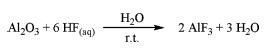 Do suspenzie Al203 sa za intenzívneho miešania pri teplote miestnosti prikvapká kyselina fluorovodíková. Následne sa tuhý oxid úplne rozpustí. Výsledný číry roztok sa mieša počas dní pri teplote miestnosti. Počas tejto doby sa biele pevné precipitáty oddelia od rozpúšťadla, premyjú sa vodou a následne sa vysušia. Po spracovaní v muflovej peci pri požadovanej teplote kalcinácie sa získa fluorid hlinitý. 3) Alkoxid hlinitý s nevodným roztokom HF4 Alkoxid hlinitý, Al(OR)3 (R=Me, Et, iPr alebo tBu), reaguje s nevodným roztokom HF v organickom rozpúšťadle. Reakcia prebieha v stave sól-gél. Po starnutí vzniká pevná látka, ktorá sa usadzuje. Pevná látka sa oddelí odstredením a vysuší sa vo vákuu. Potom sa použije fluorácia v plynnej fáze vysušeného gélu, aby sa získal fluorid hlinitý. |
| Aplikácia | Fluorid hlinitý je jednou z najdôležitejších prísad pri priemyselnej výrobe hliníka. Použitie fluoridu hlinitého môže znížiť teplotu topenia kryolitu a zlepšiť fyzikálne a chemické vlastnosti elektrolytu. Pri výrobe hliníka sa oxid hlinitý rozpúšťa v roztoku kryolitu. Prechodom elektrického prúdu cez roztok vzniká hliník. Napriek tomu sa roztok kryolitu topí pri teplote asi 1000 stupňov. Keď sa pridá fluorid hlinitý, môže dôjsť k elektrolýze v kryolitovom roztoku pri teplote o 40-60 stupňa nižšej, čím sa zníži množstvo energie potrebné na výrobu hliníka.5 Fluorid hlinitý sa používa ako bariérová vrstva na spomalenie oxidácie hliníkových zrkadiel. 6 Používa sa ako tavivo do keramických glazúr a emailov, pri výrobe kremičitanu hlinitého a ako katalyzátor. Komplexy fluoridu hlinitého s proteínmi možno použiť na štúdium mechanistických aspektov reakcií prenosu fosforu v biológii, ktoré majú zásadný význam, pretože anhydridy kyseliny fosforečnej, ako je ATP a GTP, riadia väčšinu reakcií zapojených do metabolizmu, rastu a diferenciácie.8 Fluorid hlinitý sa spolu s fluoridom zirkoničitým používa na výrobu fluorohlinitých skiel. V poľnohospodárstve môže byť fluorid hlinitý použitý na inhibíciu fermentácie. Fyzikálny naparovaný fluorid hlinitý možno použiť ako tenký optický film s nízkym indexom indexu v situáciách, keď sa vyžaduje veľká UV transparentnosť.1 |
| Toxikologické štúdie | Orálna smrteľná dávka (LD50) fluoridu hlinitého pre zvieratá je 0,1 g/kg. Fluorid hlinitý je menej toxický ako väčšina fluoridov kvôli jeho miernej rozpustnosti vo vode. Vystavenie vysokej koncentrácii fluoridu hlinitého spôsobuje hypokalciémiu. Vdýchnutie a požitie fluoridu hlinitého má za následok typické príznaky otravy fluoridom. Symptómy ťažkej otravy zahŕňajú dýchavičnosť, prekrvenie pľúc, svalové kŕče a kŕče.8 Akútne (krátkodobé) toxické účinky môžu zahŕňať úhyn zvierat, vtákov alebo rýb a úhyn alebo nízky rast rastlín. Akútne účinky sa pozorujú 2 až 4 dni po vystavení zvierat alebo rastlín fluoridu hlinitému. Chronické (dlhodobé) toxické účinky môžu zahŕňať skrátenú dĺžku života, reprodukčné problémy, nižšiu plodnosť a zmeny vzhľadu alebo správania u exponovaných zvierat. |
| Bezpečnostné opatrenia | Fluorid hlinitý je nehorľavá tuhá látka. Je však nekompatibilný s mnohými inými komoditami vrátane chemicky aktívnych kovov (napr. draslík a sodík), kyselinami a kyslými výparmi. Kontakt môže spôsobiť požiar alebo výbuch. Pri zahrievaní sa môžu uvoľňovať toxické výpary fluoridu, vrátane extrémne toxického fluorovodíka. |
| Referencie |
https://en.wikipedia.org/wiki/Alumínium_fluorid John Karlström, model reaktora na výrobu fluoridu hlinitého W. Kleist, C. Häßner, O. Storcheva, K. Köhler, Jednoduchá syntéza fluoridu hlinitého s vysokým povrchom vo vodnej fáze a jeho objemová a povrchová štruktúra, Inorganica Chimica Acta, 2006, zv. 359, str. 4851-4854 SK Ruediger, U. Groß, M. Feist, H A. Proscott, SC Shekar, SI Troyanov, E. Kemnitz, Nevodná syntéza mechanistického skúmania fluoridea hliníka s vysokým povrchom, Journal of Materials Chemistry, 2005, zv. 15, str. 588-597 https://info.noahtech.com R. Elaish, M. Curioni, K. Gowers, A. Kasuga, H. Habazaki, T. Hashimoto, P. Skeldon, Elelctrochimica Acta, 2017, roč. 245, str. 854-862 Alfred Wittinghofer, Mechanika signalizácie: Fluorid hlinitý pre molekulu roka, 1997, zv. 7, str. R682-R685 Jeffrey Wayne Vincoli, Riadenie rizík pre nebezpečné chemikálie, Bund 1, 1996, ISBN 1-56670-200-3 |
| Chemické vlastnosti | Fluorid hlinitý je biely prášok alebo granule bez zápachu. |
| Chemické vlastnosti | Fluorid hlinitý, AlF3, je bezvodý kryštalický prášok s teplotou topenia 1291 °C. Fluorid hlinitý (hydratovaný), AlF3·31/2H20 je biely kryštalický prášok, ktorý je nerozpustný vo vode. |
| Využitie | Výroba hliníka na zníženie bodu topenia a zvýšenie vodivosti elektrolytu, tavivo do keramických glazúr a emailov, výroba kremičitanu hlinitého, katalyzátor. |
| Využitie | Fluorid hlinitý sa používa na výrobu hliníka s nízkou teplotou topenia, ako tavivo v keramických glazúrach a bielych smaltoch a ako katalyzátor pri chemických reakciách. |
| Využitie | V keramike, ako tavivo v metalurgii, pri výrobe hliníka, ako inhibítor fermentácie, ako katalyzátor v organických reakciách Fluorid hlinitý sa používa v procese tavenia na zníženie teploty topenia elektrolytov, výroba kremičitanov hlinitých, rafinácia hliníkového odpadu, výroba špeciálnych žiaruvzdorné výrobky a v sklárskom priemysle ako plnivo. Používa sa ako prísada taviva na odstránenie horčíka. |
| Všeobecný popis | Biely prášok alebo granule bez zápachu. Hustejšie ako voda. Rozpustnosť vo vode pri 25 stupňoch sa rovná 0,559 g / 100 ml. |
| Reakcie vzduchu a vody | Mierne rozpustný vo vode |
| Profil reaktivity | Fluorid hlinitý pri zahriatí na sublimačné podmienky uvoľňuje toxické výpary fluoridu [USCG, 1999]. |
| Nebezpečenstvo | Silne dráždi tkanivo. |
| Zdravotné nebezpečenstvo | AKÚTNE: podráždenie dýchacích ciest; možné krvácanie z nosa alebo vracanie; CHRONICKÁ: zhoršuje bronchitídu/astmu; zvýšená hustota kostí. |
| Nebezpečenstvo požiaru | Špeciálne nebezpečenstvá spaľovacích produktov: Pri zahrievaní do sublimačných podmienok sa uvoľňujú toxické výpary fluoridu |
| Horľavosť a výbušnosť | Nehorľavý |
| Bezpečnostný profil | Jed pri požití. Stredne toxický pri subkutánnom podaní. Silne dráždiace oči. Prudko citlivý na nárazy pri kontakte s Na a K. Pri zahriatí až do rozkladu uvoľňuje toxické výpary F-. Pozri tiež FLUORIDY a ZLÚČENINY HLINÍKA. |
| Potenciálne vystavenie | Používa sa ako súčasť elektrolytu, z ktorého sa vyrába kovový hliník; pri výrobe keramiky, smaltov, kremičitanu hlinitého; ako tavivo v metalurgii; ako inhibítor fermentácie |
| Doprava | UN3260 Žieravá tuhá látka, kyslá, anorganická, nie, Trieda nebezpečnosti: 8; Štítky: 8-Korozívny materiál, vyžaduje sa technický názov. UN3077 Látky nebezpečné pre životné prostredie, tuhé, nie, Trieda nebezpečnosti: 9; Štítky: 9-Rôzny nebezpečný materiál, vyžaduje sa technický názov. |
| Nekompatibility | Prudko reaguje s draslíkom alebo sodíkom |
| Likvidácia odpadu | Neutralizujte sódou; pridajte hasené vápno; necháme odstáť 24 hodín. Preneste kal do čističky odpadových vôd. |
| Produkty a suroviny na prípravu fluoridu hlinitého |
| Suroviny | Sulfuric acid-->Sodium carbonate-->Hydrogen fluoride-->Aluminum hydroxide-->Hexafluorosilicic acid-->Calcium fluoride-->PHOS ROCK FERTILIZER IN BULK-->Methylene Blue trihydrate-->Kyselina kremičitá |
| Prípravné produkty | Fluorohlinitan draselný |
Populárne Tagy: fluorid hlinitý, Čína výrobcovia fluoridu hlinitého, dodávatelia, továreň
Tiež sa vám môže páčiť
Zaslať požiadavku


