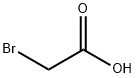
| Chemické vlastnosti |
BELÁ AŽ SVETLOŽLTÁ KRYŠTALICKÁ HMOTA |
| Využitie |
Organická syntéza, úbytok citrusových plodov pri zbere. |
| Využitie |
Kyselina brómoctová sa používa v organickej syntéze a ako alkylačné činidlo. Používa sa tiež ako biochemikália na výskum proteomiky. Je to dôležitá surovina a medziprodukt používaný v organickej syntéze, liečivách, farbivách a agrochemikáliách. |
| Využitie |
Kyselina brómoctová sa používa hlavne naN-terminálna bromoacylácia peptidov viazaných na živicu.
Môže sa použiť aj:Syntetizovať (Z)-2-(cyklookt-4-en-1-yloxy)octová kyselina.
Na syntézu -brómfenylacetamidu.
Na konverziu aromatických tiosemikarbazónov na tiazolylhydrazóny.
|
| Všeobecný popis |
Vodný roztok. |
| Reakcie vzduchu a vody |
Rozpustný vo vode. |
| Profil reaktivity |
Karboxylové kyseliny, ako je KYSELINA BROMOCETOVÁ, poskytujú vodíkové ióny, ak je prítomná báza, ktorá ich prijíma. Reagujú týmto spôsobom so všetkými zásadami, organickými (napríklad amíny) aj anorganickými. Ich reakcie so zásadami, nazývané „neutralizácie“, sú sprevádzané uvoľňovaním značného množstva tepla. Neutralizáciou medzi kyselinou a zásadou vzniká voda plus soľ. Karboxylové kyseliny so šiestimi alebo menej atómami uhlíka sú voľne alebo mierne rozpustné vo vode; tie s viac ako šiestimi uhlíkmi sú mierne rozpustné vo vode. Rozpustná karboxylová kyselina disociuje vo vode do určitej miery za vzniku vodíkových iónov. pH roztokov karboxylových kyselín je preto menšie ako 7.0. Mnohé nerozpustné karboxylové kyseliny rýchlo reagujú s vodnými roztokmi obsahujúcimi chemickú bázu a rozpúšťajú sa, keď neutralizácia vytvára rozpustnú soľ. Karboxylové kyseliny vo vodnom roztoku a kvapalné alebo roztavené karboxylové kyseliny môžu reagovať s aktívnymi kovmi za vzniku plynného vodíka a soli kovu. Takéto reakcie sa v zásade vyskytujú aj pre tuhé karboxylové kyseliny, ale sú pomalé, ak pevná kyselina zostáva suchá. Dokonca aj "nerozpustné" karboxylové kyseliny môžu absorbovať dostatok vody zo vzduchu a dostatočne sa rozpustiť v kyseline brómoctovej na koróziu alebo rozpustenie železných, oceľových a hliníkových častí a nádob. Karboxylové kyseliny, podobne ako iné kyseliny, reagujú s kyanidovými soľami za vzniku plynného kyanovodíka. Reakcia je pomalšia pre suché, pevné karboxylové kyseliny. Nerozpustné karboxylové kyseliny reagujú s roztokmi kyanidov a spôsobujú uvoľnenie plynného kyanovodíka. Horľavé a/alebo toxické plyny a teplo vznikajú reakciou karboxylových kyselín s diazozlúčeninami, ditiokarbamátmi, izokyanátmi, merkaptánmi, nitridmi a sulfidmi. Karboxylové kyseliny, najmä vo vodnom roztoku, tiež reagujú so siričitanmi, dusitanmi, tiosíranmi (za vzniku H2S a SO3), ditionitmi (SO2), pričom vznikajú horľavé a/alebo toxické plyny a teplo. Ich reakcia s uhličitanmi a hydrogénuhličitanmi vytvára neškodný plyn (oxid uhličitý), ale stále teplo. Podobne ako iné organické zlúčeniny môžu byť karboxylové kyseliny oxidované silnými oxidačnými činidlami a redukované silnými redukčnými činidlami. Tieto reakcie vytvárajú teplo. Je možná široká škála produktov. Podobne ako iné kyseliny, aj karboxylové kyseliny môžu iniciovať polymerizačné reakcie; podobne ako iné kyseliny často katalyzujú (zrýchľujú rýchlosť) chemických reakcií. |
| Nebezpečenstvo |
Silne dráždi pokožku a tkanivo. |
| Zdravotné nebezpečenstvo |
TOXICKÝ; vdýchnutie, požitie alebo kontakt (pokožka, oči) s výparmi, prachom alebo látkou môže spôsobiť vážne zranenie, popáleniny alebo smrť. Kontakt s roztavenou látkou môže spôsobiť vážne poleptanie pokožky a očí. Reakcia s vodou alebo vlhkým vzduchom uvoľňuje toxické, žieravé alebo horľavé plyny. Reakcia s vodou môže generovať veľa tepla, ktoré zvýši koncentráciu výparov vo vzduchu. Oheň vytvára dráždivé, žieravé a/alebo toxické plyny. Odtok z požiarnej alebo riediacej vody môže byť korozívny a/alebo toxický a spôsobiť znečistenie. |
| Nebezpečenstvo požiaru |
Horľavý materiál: môže horieť, ale nie je ľahké vznietiť. Látka bude reagovať s vodou (niektoré prudko), pričom sa uvoľnia horľavé, toxické alebo korozívne plyny a vytečie sa. Pri zahriatí môžu výpary tvoriť so vzduchom výbušné zmesi: nebezpečenstvo výbuchu vo vnútri, vonku a v kanalizácii. Väčšina pár je ťažšia ako vzduch. Budú sa šíriť po zemi a zhromažďovať sa v nízkych alebo stiesnených priestoroch (kanalizácie, pivnice, nádrže). Výpary môžu putovať k zdroju vznietenia a vzplanúť. Pri kontakte s kovmi sa môže uvoľňovať horľavý plynný vodík. Nádoby môžu pri zahriatí alebo kontaminácii vodou explodovať. |
| Horľavosť a výbušnosť |
Nehorľavý |
| Bezpečnostný profil |
Otrava požitím, intraperitoneálnou a intravenóznou cestou. Dráždi a žiera pokožku a sliznice. Boli hlásené údaje o mutácii. Pri zahrievaní do rozkladu uvoľňuje toxické výpary Br-. Pozri tiež BROMIDY. |
| Spôsoby čistenia |
Kyselina brómoctová kryštalizuje z pet éteru (b 40-60o). Dietyléterový roztok sa nechá prejsť kolónou s oxidom hlinitým a éter sa odparí pri teplote miestnosti vo vákuu. Najlepšie sa získava destiláciou z Claisenovy banky (banka ponorená do olejového kúpeľa) vybavenej izolovanou Vigreuxovou kolónou (str. 11) a zachytáva sa frakcia b 108-110o/30 mm. Je citlivý na svetlo a vlhkosť. [Natelson & Gottfried Org Synth Coll zv. III 381 1955, Beilstein 2 IV 526.] LACHRYMÁTORNÉ a dráždi pokožku. |