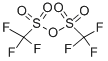
| Popis |
Anhydrid kyseliny trifluórmetánsulfónovej, tiež známy ako anhydrid kyseliny trifluórmetánsulfónovej, sa ukázal ako mimoriadne činidlo pre široký rozsah transformácií. Ako komerčne a ľahko dostupné činidlo sa široko používa v syntetickej chémii kvôli svojej vysokej elektrofilnosti. Vzhľadom na jeho vysokú afinitu k O-nukleofilom je silne uprednostňovaná reakcia s alkoholmi, karbonylmi, oxidmi síry, fosforu a jódu smerom k tvorbe zodpovedajúcich triflátov. Ako jedna z popredných odstupujúcich skupín v organickej chémii generované trifláty potom otvárajú dvere rôznym následným transformáciám, vrátane (okrem iného) substitučných reakcií, procesov krížovej väzby, redoxných reakcií a preskupení[1-2] . |
| Chemické vlastnosti |
číra bezfarebná až svetlohnedá kvapalina |
| Využitie |
Anhydrid kyseliny trifluórmetánsulfónovej je silný elektrofil používaný v chemickej syntéze na zavedenie triflylovej skupiny. |
| Využitie |
Anhydrid kyseliny trifluórmetánsulfónovej sa používa na konverziu fenolov a imínu na ester kyseliny trifluóroctovej a skupinu NTf. Je to silný elektrofil používaný na zavedenie triflylovej skupiny v chemickej syntéze. Slúži ako činidlo pri príprave alkylových a vinylových triflátov a na stereoselektívnu syntézu donorov mannosazid metyluronátu. Pôsobí ako katalyzátor glykozylácie s anomérnymi hydroxysacharidmi na prípravu polysacharidov. |
| Definícia |
ChEBI: Anhydrid kyseliny triflovej je anhydrid kyseliny organosulfónovej. Funkčne súvisí s kyselinou triflovou. |
| Profil reaktivity |
Elektrofilná aktivácia terciárnych a sekundárnych amidov anhydridom kyseliny trifluórmetánsulfónovej (Tf2O; anhydrid kyseliny rifluórmetánsulfónovej) za miernych podmienok vedie k vzniku imínium a iminotriflátu, ktoré by sa mohli použiť ako všestranné činidlá na reakciu s rôznymi C-, N-, O- a S -nukleofily na transformáciu amidovej funkcie na rôzne produkty. Iné nukleofily obsahujúce kyslík, ako sú sulfoxidy a oxidy fosforu, by tiež mohli podstúpiť nukleofilný útok s Tf20 za vzniku tioniumtriflátu, elektrofilných P-druhov a fosfóniumtriflátu. Tieto vysoko aktívne prechodné druhy by mohli ľahko podstúpiť nukleofilné substitučné reakcie pre ďalšie rôzne transformácie. Okrem toho je Tf20 vzhľadom na silné elektrofilné vlastnosti náchylný reagovať s relatívne slabými nukleofilmi, ako sú nitrilové skupiny alebo niektoré heterocyklické zlúčeniny obsahujúce dusík. Okrem toho sa Tf2O tiež používa ako účinné radikálové trifluórmetylačné a trifluórmetyltiolačné činidlo prostredníctvom uvoľňovania S02 alebo deoxygenačného procesu na syntézu trifluórmetylovaných a trifluórmetyltiolátových zlúčenín[2]. |
| Nebezpečenstvo |
Môže byť korozívny pre kovy. Škodlivý pri požití. Spôsobuje ťažké poleptanie kože a poškodenie očí. |
| Horľavosť a výbušnosť |
Nie je klasifikované |
| Syntéza |
Syntéza anhydridu kyseliny trifluórmetánsulfónovej je nasledovná:
Suchá, {{0}}}ml banka s guľatým dnom sa naplní 36,3 g. (0,242 mol) kyseliny trifluórmetánsulfónovej (Poznámka 1) a 27,3 g. (0,192 mol) oxidu fosforečného (poznámka 2). Banka sa zazátkuje a nechá sa stáť pri teplote miestnosti aspoň 3 hodiny. Počas tejto doby sa reakčná zmes zmení zo suspenzie na pevnú hmotu. Banka je vybavená krátkocestnou destilačnou hlavou a zahrieva sa najprv prúdom horúceho vzduchu z teplovzdušnej pištole a potom plameňom z malého horáka.Banka sa zahrieva, kým už neprestane destilovať anhydrid kyseliny trifluórmetánsulfónovej, teplota varu 82 až 115 stupňov, čím sa získa 28,4 až 31,2 g. (83–91 %) anhydridu, bezfarebná kvapalina. Hoci je tento produkt dostatočne čistý na použitie v nasledujúcom kroku, zostávajúca kyselina sa môže z anhydridu odstrániť nasledujúcim postupom. Suspenzia 3,2 g. oxidu fosforečného v 31,2 g. surového anhydridu sa mieša pri teplote miestnosti v uzavretej banke počas 18 hodín. Potom, čo bola reakčná banka vybavená krátkocestnou destilačnou hlavou, zahrieva sa v olejovom kúpeli, čím sa získa 0,7 g. predbehnutia, bp 74–81 stupňov, po ktorom nasledovalo 27,9 g. čistého anhydridu kyseliny trifluórmetánsulfónovej, teplota varu 81 až 84 stupňov.

|
| skladovanie |
Skladujte na chladnom, suchom, dobre vetranom mieste. Citlivý na vlhkosť. |
| Spôsoby čistenia |
Môže sa čerstvo pripraviť z bezvodej kyseliny (11,5 g) a P2O5 (11,5 g alebo polovica tejto hmotnosti) odstavením pri teplote miestnosti na 1 hodinu, oddestilovaním prchavých produktov a potom destiláciou cez krátku Vigreuxovu kolónu. Ľahko sa hydrolyzuje H2O a po niekoľkých dňoch sa značne rozkladá, čím sa uvoľňuje SO2 a vzniká viskózna kvapalina. Skladujte v suchu pri nízkych teplotách. [Burdon a kol. J Chem Soc 2574 1957, Beard a kol. J Org Chem 38 373 1973, Beilstein 3 IV 35.] |
| Referencie |
[1] Haoqi Zhang. "Anhydrid kyseliny trifluórmetánsulfónovej v aktivácii amidu: výkonný nástroj na vytváranie heterocyklických jadier." TCIMAIL (2021).
[2] Dr. Qixue Qin, prof. Dr. Ning Jiao, Zengrui Cheng. "Nedávne aplikácie anhydridu kyseliny trifluórmetánsulfónovej v organickej syntéze." Angewandte Chemie 135 10 (2022). |