
Predstavenie výrobku
| 4-Základné informácie o chlóranilíne |
| Meno Produktu: | 4-Chlóranilín |
| Synonymá: | AKOS BBS-00003661;4-chlóranilínový roztok;P-chlórlanín;PARA-CHLORANILÍN;4-CHLORANILÍN;4-aminochlórbenzén;4-chlóranilín;4- chloranilín (česky) |
| CAS: | 106-47-8 |
| MF: | C6H6ClN |
| MW: | 127.57 |
| EINECS: | 203-401-0 |
| Kategórie produktov: | 2002/61/EC;Alfa triedenie;Arylamíny MAK III, kategória 2Prchavé/poloprchavé látky;C;ALfabetické;CHmetódy špecifické;Amíny;C2 až C6;Zlúčeniny dusíka;Európske spoločenstvo: ISO a DIN;Špecifické pre metódu;Oeko-Tex Standard 100 ;Arylamíny MAK III, kategória 2 abecedne;Arylamíny MAK III, kategória 2 Pesticídy a metabolity;Fluórbenzén;Anilíny, aromatické amíny a nitrozlúčeniny;ChlórViac...Close...;Analytické štandardy;Aromatické triedyChemická trieda;AromatikaChemická;Špecifické ;Halogénované;Aromáty;amín|alkylchlorid;1 |
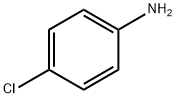
| Súbor Mol: | 106-47-8.mol |
 |
|
| 4-Chloraniline Chemical Properties |
| Bod topenia | 67-70 stupeň (dosl.) |
| Bod varu | 232 stupňov (lit.) |
| hustota | 1,43 G/CM3 |
| hustota pár | 4,4 (oproti vzduchu) |
| tlak vodnej pary | 0,15 mm Hg (25 stupňov) |
| index lomu | 1.5546 |
| Fp | 120 stupňov |
| skladovacia teplota | Skladujte pod +30 stupňom . |
| rozpustnosť | 2.2g/l |
| PKA | 4,15 (pri 25 stupňoch) |
| formulár | Kryštalická tuhá látka |
| Špecifická gravitácia | 1.2417 |
| farba | Béžová až hnedofialová |
| PH | 6,9 (1 g/l, H2O, 20 stupňov) |
| Zápach | Sladký |
| Rozsah PH | 6,9 pri 1,{3}} g/l pri 20 stupňoch |
| Rozpustnosť vo vode | 0,3 g/100 ml (20 ºC) |
| Merck | 14,2118 |
| BRN | 471359 |
| Konštantný Henryho zákon | 1,07 pri 25 stupňoch (vypočítané, Howard, 1989) (x 10-5atm?m3/mol) |
| Stabilita: | Stabilný. Horľavý. Nekompatibilný so silnými oxidačnými činidlami, kyselinami, chloridmi kyselín, anhydridmi kyselín, chlórmravčanmi, kyselinou dusitou. Môže byť citlivý na svetlo. |
| LogP | 1,83 pri 25 stupňoch |
| Referencia databázy CAS | 106-47-8(Referencia databázy CAS) |
| NIST Chémia Referencie | p-chlóranilín (106-47-8) |
| IARC | 2B (zv. 57) 1993 |
| Systém registra látok EPA | p-chlóranilín (106-47-8) |
| Bezpečnostné informácie |
| Kódy nebezpečnosti | T,N,F |
| Výkazy o riziku | 45-23/24/25-43-50/53-52/53-39/23/24/25-11-51/53 |
| Bezpečnostné vyhlásenia | 53-45-60-61-36/37-16-7 |
| RIDADR | OSN 2018 6.1/PG 2 |
| WGK Nemecko | 3 |
| RTECS | BX0700000 |
| F | 8-10-23 |
| Teplota samovznietenia | 685 stupňov |
| Poznámka k nebezpečenstvu | Toxický/možný karcinogén |
| TSCA | Áno |
| Trieda nebezpečnosti | 6.1 |
| Baliaca skupina | II |
| HS kód | 29214210 |
| Údaje o nebezpečných látkach | 106-47-8(Údaje o nebezpečných látkach) |
| Toxicita | LD50 perorálne u potkanov: 0,31 g/kg (Smyth) |
| Informácie o karte bezpečnostných údajov |
| Poskytovateľ | Jazyk |
|---|---|
| 4-Chlórbenzénamín | Angličtina |
| ACROS | Angličtina |
| SigmaAldrich | Angličtina |
| ALFA | Angličtina |
| 4-Použitie a syntéza chlóranilínu |
| Popis | p-Chlóranilín, 1-amino-4- chlórbenzén, je pri izbovej teplote biela až svetlojantárová kryštalická tuhá látka. Používa sa ako medziprodukt pre pesticídy, liečivá, pigmenty a farbivá. Výroba je podobná výrobe m-chlóranilínu. |
| Chemické vlastnosti | 4-Chlóranilín je bezfarebná až slabo jantárovo sfarbená kryštalická pevná látka s miernym aromatickým zápachom. Je rozpustný v horúcej vode a organických rozpúšťadlách. 4-Chlóranilín má mierny tlak pár a rozdeľovací koeficient n-oktanol/voda. Rozkladá sa v prítomnosti svetla a vzduchu a pri zvýšených teplotách. |
| Fyzikálne vlastnosti | Žltobiela tuhá látka s miernym, sladkastým zápachom. Prahová koncentrácia zápachu je 287 ppm (citované, Keith a Walters, 1992). |
| Využitie | 4-Chlóranilín je dôležitou surovinou pri výrobe poľnohospodárskych chemikálií, azofarbív a pigmentov, kozmetiky a farmaceutických produktov. Používa sa ako medziprodukt pri výrobe chromofóru AS-LB, ako aj vo farmaceutických medziproduktoch, ako je chlordiazepoxid a tinktúra fena. Je tiež medziproduktom pre herbicíd Anilofos, insekticíd chlórbenzuron a regulátor rastu rastlín Inabenfide. |
| Definícia | ChEBI: 4-chlóranilín je chlóranilín, v ktorom je atóm chlóru para k anilínovej aminoskupine. Je to chlóranilín a člen monochlórbenzénov. |
| Aplikácia | 4-Chlóranilín je dôležitým stavebným kameňom používaným v chemickom priemysle na výrobu liekov a farbív. Niektoré benzodiazepínové lieky používajú pri výrobe 4-chlóranilín. |
| Príprava | syntéza 4-chlóranilínu: ako surovina sa používa p-chlórnitrobenzén, ako katalyzátor sa používa Raneyov nikel, ako rozpúšťadlo sa používa etanol, reakčná teplota je 50-70 stupeň, tlak hydrogenácie je 3.{{4} },55 MPa a stredné pH=5-6 podmienky, vykonajte katalytickú hydrogenačnú reakciu, aby ste získali 4-chlóranilín. |
| Syntéza referencie | Journal of the American Chemical Society, 99, s. 98, 1977DOI:10.1021/ja00443a018 Synthesis, s. 48, 1987DOI: 10.1055/s-1987-27838 |
| Všeobecný popis | P-chlóranilín sa javí ako biela alebo svetložltá pevná látka. Teplota topenia 69,5 stupňa. |
| Reakcie vzduchu a vody | Nerozpustný v studenej vode. Rozpustný v horúcej vode [Hawley]. |
| Profil reaktivity | 4-Chlóranilín je nekompatibilný s oxidačnými činidlami. Tiež nekompatibilný s kyselinami, chloridmi kyselín, anhydridmi kyselín a chlórformiátmi. Počas vysokoteplotnej destilácie podlieha exotermickému rozkladu. Nekompatibilný s kyselinou dusitou. |
| Nebezpečenstvo | Toxický pri vdýchnutí a požití. Možný karcinogén. |
| Hazard so zdravím | Vdýchnutie alebo požitie spôsobuje modrasté sfarbenie nechtov, pier a uší, čo svedčí o cyanóze; bolesť hlavy, ospalosť a nevoľnosť, po ktorých nasleduje bezvedomie. Kvapalina sa môže absorbovať cez pokožku a spôsobiť podobné príznaky. Kontakt s očami spôsobuje podráždenie. |
| Nebezpečenstvo ohňa | Špeciálne nebezpečenstvá horľavých produktov: Pri požiari sa môže vytvárať dráždivý a jedovatý chlorovodík a oxidy dusíka. |
| Horľavosť a výbušnosť | Horľavý |
| Bezpečnostný profil | Potvrdený karcinogén s experimentálnymi neoplastigénnymi a tumorigénnymi údajmi. Otrava požitím, vdýchnutím, sh kontaktom, subkutánnou a intravenóznou cestou. Silne dráždi pokožku a oči. Boli hlásené údaje o mutácii. Pri zahrievaní do rozkladu uvoľňuje toxické výpary Cland NOx. Pozri tiež ANILÍNOVÉ FARBIVÁ |
| Environmentálny osud | Biologické.V anaeróbnom médiu baktérie Paracoccus sp. konvertoval 4-chlóranilín na 1,3-bis(p-chlórfenyl)triazén a 4-chlóracetanilid s výťažkami produktu 80 a 5 %, v tomto poradí (Minard a kol., 1977). V poľnom experimente [14C]4-chlóranilín sa aplikoval na pôdu v hĺbke 10 cm. Po 20 týždňoch sa v pôde obnovilo 32,4 % aplikovaného množstva. Identifikované metabolity zahŕňajú 4-chlórformanilid, 4-chlóracetanilid, 4-chlórnitrobenzén, 4- chlórnitrózobenzén, 4,4'-dichlórazoxybenzén a 4,4'-dichlórazobenzén (Freitag et al. , 1984). Pôda.4-Chlóranilín sa kovalentne viaže s humátmi v pôde za vzniku chinoidných štruktúr, po ktorých nasleduje oxidácia za vzniku chinoidného kruhu substituovaného dusíkom. S jednou humínovou zlúčeninou sa stanovil polčas reakcie 13 minút (Parris, 1980). Katechol, monomér humínovej kyseliny, reagoval s 4-chlóranilínom za vzniku 4,5-bis(4-chlórfenylamino)-3,5-cyklohexadiénu-1, 2-dion (Adrian a kol., 1989). Fotolytické.Under artificial sunlight, river water containing 2–5 ppm 4-chloroaniline photodegraded to 4-aminophenol and unidentified polymers (Mansour et al., 1989). Photooxidation of 4-chloroaniline (100 μM) in air-saturated water using UV light (λ >290 nm) produced 4-chloronitrobenzene and 4-chloronitrosobenzene. About 6 h later, 4-chloroaniline completely reacted leaving dark purple condensation products (Miller and Crosby, 1983). In a similar study, irradiation of an aqueous solution in the range of 290–350 nm resulted in the formation of the intermediate 4-iminocyclohexa-2,5-dienylidene (Othmen et al., 2000). A carbon dioxide yield of 27.7% was achieved when 4-chloroaniline adsorbed on silica gel was irradiated with light (λ >290 nm) počas 17 hodín (Freitag a kol., 1985). rýchlostná konštanta 8,3 x 10-11cm3/molecule?sec bola uvedená pre reakciu 4- chlóranilínu a OH radikálov vo vzduchu v plynnej fáze (Wahner a Zetzsch, 1983). Chemické/Fyzikálne.4-Chlóranilín nebude hydrolyzovať v rozumnej miere (Kollig, 1993). Pizzigallo a kol. (1998) skúmali reakciu 4-chlóranilínu s oxidom železitým a dvoma formami oxidu manganičitého [birnessit (δ-MnO2) a pyrolusit (MnO2)] v rozsahu pH 4–8 pri 25 stupňoch . Reakčná rýchlosť 4-chlóranilínu bola v poradí birnessit > pyrolusit > oxid železitý. Pri pH 4.{10}} bola reakcia s birnessitom taká rýchla, že sa nedala určiť. Polčasy reakcie 4-chlóranilínu s pyroluzitom a oxidom železitým boli 383 a 746 minút. Rýchlosť reakcie sa znižovala so zvyšujúcim sa pH. Jedinými oxidačnými zlúčeninami identifikovanými pomocou GC/MS boli 4,4′-dichlórazobenzén a 4-chlór-4′-hydroxydifenylamín. |
| Spôsoby čistenia | Anilín sa kryštalizuje z MeOH, petroléteru (b 30-60o) alebo 50 % vodného EtOH, potom *benzén/petroléter (b 60-70o) a potom sa vysuší vo vákuovom exsikátore. Môže sa destilovať vo vákuu (b 75-77o/3 mm). Sublimuje vo veľmi vysokom vákuu. Acetát kryštalizuje z vodného MeOH (m 178o, 180o) alebo EtOH alebo AcOH (m 173-174o) a má b 331,3o/760 mm. [Beilstein 12 III 1325, 12 IV 1116.] |
| 4-Výrobky a suroviny na prípravu chlóranilínu |
| Suroviny | Iron-->Nickel-->4-Chloronitrobenzene-->Nikel aluMinuM |
| Prípravné produkty | N-(2-[4-(4-CHLOROPHENYL)PIPERAZIN-1-YL]ETHYL)-3-METHOXYBENZAMIDE-->2-Amino-5-chlorobenzophenone-->2,6-Dichlorobenzothiazole-->chlorbenzuron-->cintofen-->Lorcainide-->3-Chlorophenol-->FLURAZEPAM-->Anilofos-->Tenidap-->Efavirenz-->6-CHLORO-2-(TRIFLUOROMETHYL)QUINOLINE-4-CARBOXYLIC ACID-->Nitrazepam-->5-AMINO-1-(4-CHLOROPHENYL)-1H-PYRAZOLE-4-CARBONITRILE-->6-CHLORO-2-METHYLQUINOLINE-->Diflubenzuron-->1-CHLORO-4-ISOCYANOBENZENE-->N-(4-chlorophenyl)-1-isopropylpiperidin-4-amine-->4-(4-(Chlorophenyl)imino)-1-isopropyl piperidine-->2-Amino-5-chloro-2'-fluorobenzophenone-->N-(4-chlorophenyl)-2-hydroxy-9H-carbazole-3-carboxamide-->4-CHLORO-(N-BOC)ANILINE 97-->1-(4-Chlorophenyl)piperazine-->2-amino-5-chloro-diphenyl methanol-->4-Chlorophenyl isocyanate-->Naphthol AS-E-->polyaniline synthesized by means of condensation polymerization-->imidazol-2-ylamine sulphate-->4-Chlorophenylhydrazine-->5-Chloroorthanilic acid-->Chlorhexidine Diacetate-->Cloflucarban-->Chlórhexidín diacetát |
Populárne Tagy: 4-chlóranilín, Čína 4-výrobcovia chlóranilínu, dodávatelia, továreň
Dvojica: 4-Chlórfenylizokyanát
Ďalšie: Difenylsulfón
Tiež sa vám môže páčiť
Zaslať požiadavku







