
Predstavenie výrobku
| Pyridín Základné informácie |
| Chemická štruktúra Chemické vlastnosti Výroby Použitie Informácie o toxicite Odkazy na riziká |
| Meno Produktu: | Pyridín |
| Synonymá: | pyridínkarboxylová kyselina,2-(4,5-dihydro-4-metyl-4-(1-metyletyl)-5-oxo-1h-imidazol{ {9}}yl)-5-metyl;pyridínkarboxylová kyselina,2-(4,5-dihydro-4-metyl-4-(1-metyletyl){{ 17}}oxo-1h-imidazol-2-yl)-5-metyl,monoamónna soľ;Rcra číslo odpadu U196;rcrawastenumberu196;FEMA 2932;FEMA 2966;FEMA ČÍSLO 2966;azabenzén |
| CAS: | 110-86-1 |
| MF: | C5H5N |
| MW: | 79.1 |
| EINECS: | 203-809-9 |
| Kategórie produktov: | Fľaše z jantárového skla;NMR;Fľaše s rozpúšťadlami;Rozpúšťadlo podľa aplikácie;Rozpúšťadlo podľa typu;Možnosti balenia rozpúšťadla;Biotech SolventsRozpúšťadlá;Fľaše s rozpúšťadlami;Rozpúšťadlá;Určite/Utesniť? Fľaše;Spektrofotometrická kvalita;Spektrofotometrické rozpúšťadlá;Rozpúšťadlá pre spektroskopiu (IR;UV/Vis);Organostany;Tributylcín;Chémia;PS;Alpha Sort;Prchavé/poloprchavé;Fľaše z jantárového skla;ReagentPlus(R) SolventagentPlus Products(R;ReagentPlus®) ;ACS Grade Solvents;CHROMASOLV PlusCHROMASOLV Solvents (HPLC, LC-MS);CHROMASOLV® Plus;LC-MS Plus a Gradient;Abecedné;P;PU - PZ;Pyridín;Organohalidy;Ester bóru;Organobóry;Organosilan;ACS; -Veľkoobjemové rozpúšťadlá;Rozpúšťadlá triedy ACS;Kanystry z uhlíkovej ocele so závitmi NPT;Rozpúšťadlá pre vratné nádoby;Rozpúšťadlá ACS a reagencie;ReagentPlus;ReagentPlus produkty triedy rozpúšťadiel;Biotech rozpúšťadlá;Utesňovacie fľaše;Kód ACS;Analytické činidlá pre všeobecné použitie;Analytické činidlá pre všeobecné použitie ;Analytická/chromatografia;Multi-Compendial;Puriss pa;Puriss pa ACS;Fľaše potiahnuté PVC;Hliníkové fľaše;CHROMASOLV Plus;Chromatografické činidlá &;HPLC &;HPLC Plus Grade Solvents (CHROMASOLV);HPLC/UHPLCV rozpúšťadlá (CHROMASOLV); Rozpúšťadlá (CHROMASOLV);Rozpúšťadlá triedy ACS;Kanistry z uhlíkovej ocele so závitmi NPT;Poloobjemové rozpúšťadlá;Halogénované;Fluórované;Stavebné bloky;Kyselina boritá;Karboxy;Alkoxy;Analytické činidlá na všeobecné použitie;OP, Puriss pa;Puriss pa;OP , Puriss pa ACS;Puriss pa ACS;Hliníkové fľaše;Abecedné zoznamy;Príchute a vône;OP;Rozpúšťadlá spektrofotometrickej kvality;Rozpúšťadlá spektrofotometrickej triedy;Fľaše potiahnuté PVC;ReagentPlus(R) Rozpúšťadla };bc0001 |
| Súbor Mol: | 110-86-1.mol |
 |
|
| Chemické vlastnosti pyridínu |
| Bod topenia | -42 stupeň (dosl.) |
| Bod varu | 115 stupňov (lit.) |
| hustota | 0,978 g/ml pri 25 stupňoch (lit.) |
| hustota pár | 2,72 (v porovnaní so vzduchom) |
| tlak vodnej pary | 23,8 mm Hg (25 stupňov) |
| index lomu | n20/D 1,509 (lit.) |
| FEMA | 2966|PYRIDINE |
| Fp | 68 stupňov F |
| skladovacia teplota | Skladujte pri teplote +5 až +30 stupňoch . |
| rozpustnosť | H2O: v súlade |
| pka | 5,25 (pri 25 stupňoch) |
| formulár | Kvapalina |
| farba | bezfarebný |
| Zápach | Nevoľný zápach zistiteľný pri 0,23 až 1,9 ppm (priemerne=0,66 ppm) |
| Relatívna polarita | 0.302 |
| PH | 8,81 (H20, 20 stupňov) |
| limit výbušnosti | 12.4% |
| Prahová hodnota zápachu | 0.063 str./min |
| Typ zápachu | rybí |
| Rozpustnosť vo vode | Miešateľný |
| Bod mrazu | -42 stupeň |
| λmax | λ: 305 nm Amax: 1.00 λ: 315 nm Amax: 0,15 λ: 335 nm Amax: 0,02 λ: {{0}} nm Amax: 0,01 |
| Merck | 14,7970 |
| BRN | 103233 |
| Konštantný Henryho zákon | 18,4 pri 30 stupňoch (headspace-GC, Chaintreau a kol., 1995) |
| Expozičné limity | TLV-TWA 5 ppm (-15 mg/m3) (ACGIH, MSHA a OSHA); STEL 10 ppm (ACGIH), IDLH 3600 ppm (NIOSH). |
| Dielektrická konštanta | 12,5 (20 stupňov) |
| Stabilita: | Stabilný. Horľavý. Nekompatibilné so silnými oxidačnými činidlami, silnými kyselinami. |
| InChIKey | JUJWROOIHBZHMG-UHFFFAOYSA-N |
| LogP | 0,64 pri 20 stupňoch |
| Referencia databázy CAS | 110-86-1(Referencia databázy CAS) |
| NIST Chemistry Reference | Pyridín (110-86-1) |
| IARC | 2B (zv. 77, 119) 2019 |
| Systém registra látok EPA | Pyridín (110-86-1) |
| Bezpečnostné informácie |
| Kódy nebezpečnosti | T, N, F, Xn |
| Výkazy o riziku | 11-20/21/22-39/23/24/25-23/24/25-52-36/38 |
| Bezpečnostné vyhlásenia | 36/37/39-38-45-61-28A-26-28-24/25-22-36/37-16-7 |
| OEB | A |
| OEL | TWA: 5 ppm (15 mg/m3) |
| RIDADR | OSN 1282 3/PG 2 |
| WGK Nemecko | 2 |
| RTECS | 8400000 UR |
| F | 3-10 |
| Teplota samovznietenia | 482 stupňov |
| Poznámka k nebezpečenstvu | Veľmi horľavý/škodlivý |
| TSCA | Áno |
| HS kód | 2933 31 00 |
| Trieda nebezpečnosti | 3 |
| PackingGroup | II |
| Údaje o nebezpečných látkach | 110-86-1(Údaje o nebezpečných látkach) |
| Toxicita | LD50 orálne u potkanov: 1,58 g/kg (Smyth) |
| IDLA | 1, 000 str./min |
| Informácie o karte bezpečnostných údajov |
| Poskytovateľ | Jazyk |
|---|---|
| SigmaAldrich | Angličtina |
| ACROS | Angličtina |
| ALFA | Angličtina |
| Použitie a syntéza pyridínu |
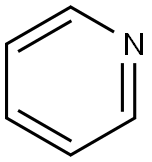
| Chemická štruktúra | Pyridín je bázická heterocyklická organická zlúčenina s chemickým vzorcom C5H5N. Štruktúrne je príbuzný benzénu, pričom jedna metínová skupina (=CH−) je nahradená atómom dusíka. Pyridínový kruh sa vyskytuje v mnohých dôležitých zlúčeninách vrátane azínov a vitamínov niacínu a pyridoxínu.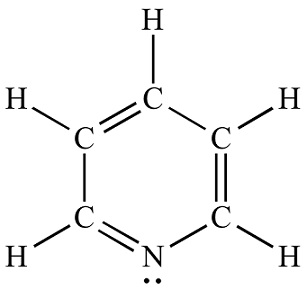 Štruktúra pyridínu Lewisa |
| Chemické vlastnosti | Pyridín je bezfarebná horľavá kvapalina so silným a nepríjemným rybím zápachom. Pyridín |
| Produkcie | 2.1 Oddelenie od dechtu Pyridínové zásady sú zložkou dechtov. Boli izolované z uhoľného dechtu alebo uhoľného plynu predtým, ako sa ustanovili syntetické výrobné procesy. Množstvo obsiahnuté v uhoľnom dechte a uhoľnom plyne je malé a z nich izolované pyridínové zásady sú zmesou mnohých zložiek. Izolácia čistých pyridínových zásad bola teda až na niekoľko výnimiek nákladná. Dnes sa takmer všetky pyridínové bázy vyrábajú syntézou.2.2 Syntéza chihibabinu 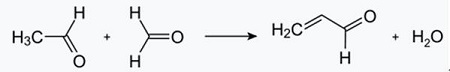 Obr. 2-1Tvorba akroleínu z acetaldehydu a formaldehydu 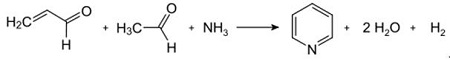 Obr. 2-2Kondenzácia pyridínu z akroleínu a acetaldehydu Chihibabin pyridínová syntéza bola opísaná v roku 1924 a stále sa používa v priemysle. Acetaldehyd a formaldehyd reagujú s amoniakom za vzniku hlavne pyridínu. Najprv sa akroleín tvorí Knoevenagelovou kondenzáciou z acetaldehydu a formaldehydu. Potom sa kondenzuje s acetaldehydom a amoniakom na dihydropyridín a potom sa oxiduje katalyzátorom v pevnom stave na pyridín. Reakcia sa zvyčajne uskutočňuje pri 350-550 °C a priestorovej rýchlosti 500-1000 h-1v prítomnosti pevného kyslého katalyzátora (napr. oxid kremičitý-oxid hlinitý). Produkt pozostáva zo zmesi pyridínu, jednoduchých metylovaných pyridínov (pikolín) a lutidínu. Získaný pyridín sa oddeľuje od vedľajších produktov vo viacstupňovom procese. 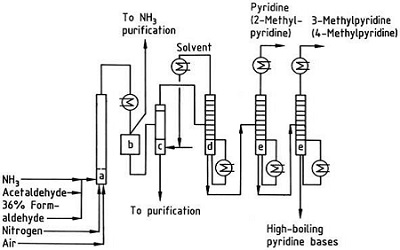 Obr. 2-3Schéma výroby pyridínu a metylpyridínu z acetaldehydu a formaldehydu s amoniakom. A) reaktor; b) zberač; c) extrakcia; d) destilácia rozpúšťadla; e) Destilácia 2.3 Dealkylácia alkylpyridínov Pyridín sa môže pripraviť dealkyláciou alkylovaných pyridínov, ktoré sa získavajú ako vedľajšie produkty pri syntézach iných pyridínov. Oxidačná dealkylácia sa vykonáva buď použitím vzduchu nad katalyzátorom na báze oxidu vanádu (V), parnou dealkyláciou na katalyzátore na báze niklu, alebo hydrodealkyláciou s katalyzátorom na báze striebra alebo platiny. S katalyzátorom na báze niklu je možné dosiahnuť výťažky pyridínu až do 93 %. 2.4 Syntéza z nitrilov a acetylénu Reakcia nitrilov s acetylénom v kvapalnej fáze sa uskutočňuje pri 120-180 °C a 0.8-2 0,5 MPa v prítomnosti organokobaltového katalyzátora a poskytuje 2-substituované pyridíny : 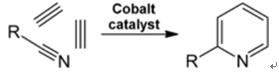 Obr. 2-4Syntéza 2-metylpyridínu z nitrilov a acetylénu Trimerizácia časti molekuly nitrilu a dvoch častí acetylénu na pyridín sa nazýva Bönnemannova cyklizácia. Pri použití acetonitrilu ako nitrilu sa získa 2-metylpyridín, ktorý možno dealkylovať na pyridín. 2.5 Syntéza z akrylonitrilu a ketónov 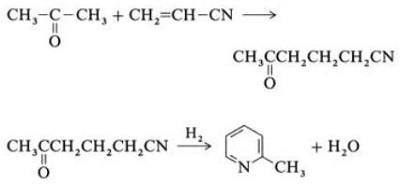 Obr. 2-5Syntéza 2-metylpyridínu z akrylonitrilu a acetónu Syntézou z akrylonitrilu a acetónu sa selektívne získa 2-metylpyridín, ktorý možno dealkylovať na pyridín. Po prvé, reakcia akrylonitrilu a acetónu, katalyzovaná primárnym alifatickým amínom, ako je izopropylamín, a slabou kyselinou, ako je kyselina benzoová, prebieha v kvapalnej fáze pri 180 °C a 2,2 MPa za vzniku 5-oxohexánnitrilu s 91 % selektivity. Konverzia akrylonitrilu je 86 %. Potom sa uskutoční cyklizácia a dehydratácia počiatočného produktu v plynnej fáze v prítomnosti vodíka na katalyzátore obsahujúcom paládium, nikel alebo kobalt pri 240 °C, čím sa získa 2-metylpyridín s výťažkom 84 %. 2.6 Syntéza z dinitrilov V reakcii v plynnej fáze nad katalyzátorom obsahujúcim nikel v prítomnosti vodíka poskytuje 2-metylglutaronitril 3-metylpiperidín, ktorý potom podlieha dehydrogenácii nad paládium-oxidom hlinitým za vzniku 3-metylpyridínu. A 3-metylpyridín môže byť tiež dealkylovaný na pyridín. 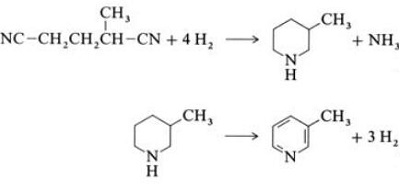 Obr. 2-6Syntéza 2-metylpyridínu z dinitrilov Uvádza sa, že jednokroková reakcia v plynnej fáze na katalyzátore obsahujúcom paládium poskytuje 3-metylpyridín v 50 % výťažku. 2.7 Biosyntéza Niekoľko derivátov pyridínu hrá dôležitú úlohu v biologických systémoch. Zatiaľ čo jej biosyntéza nie je úplne pochopená, kyselina nikotínová (vitamín B3) sa vyskytuje u niektorých baktérií, húb a cicavcov. Cicavce syntetizujú kyselinu nikotínovú oxidáciou aminokyseliny tryptofán, pričom medziprodukt, anilín, vytvára derivát pyridínu, kynurenín. Naopak, baktérie Mycobacterium tuberculosis a Escherichia coli produkujú kyselinu nikotínovú kondenzáciou glyceraldehyd 3-fosfátu a kyseliny asparágovej. 2.8 Iné metódy Etylén a amoniak reagujú v prítomnosti katalyzátora na báze paládiového komplexu za vzniku 2-metylpyridínu a MEP. Pyridín možno pripraviť z cyklopentadiénu ammoxidáciou alebo z 2-penténnitrilu cyklizáciou a dehydrogenáciou. Furfurylalkohol alebo furfural reaguje s amoniakom v plynnej fáze za vzniku pyridínu. 2-Metylpyridín sa tiež pripravuje z anilínu. |
| Využitie | 3.1 Rozpúšťadlo Pyridín (110-86-1) je polárne, zásadité, málo reaktívne rozpúšťadlo, najmä na dehydrochloračné reakcie a extrakciu antibiotík. Pri eliminačnej reakcii pôsobí pyridín ako báza eliminačnej reakcie a viaže výsledný halogenovodík za vzniku pyridíniovej soli. Pri esterifikácii a acylácii pyridín aktivuje halogenidy alebo anhydridy karboxylových kyselín. 3.2 Lieky Chemickú štruktúru pyridínu možno nájsť v rôznych liekoch, ktoré sa syntetizujú čiastočne vďaka pyridínu. Jedným príkladom je liek nazývaný esomeprazol, všeobecný názov pre Nexium. Toto je liek, ktorý sa používa na liečbu GERD alebo gastroezofageálneho refluxu. Ďalším príkladom lieku obsahujúceho pyridín je loratadín, bežnejšie známy pod obchodným názvom Claritin. Loratadín pomáha pri liečbe alergií. 3.3 Pesticídy Hlavné použitie pyridínu je ako prekurzor herbicídov paraquat a diquat. Prvý krok syntézy insekticídu chlorpyrifos pozostáva z chlorácie pyridínu. Pyridín je tiež východiskovou zlúčeninou na prípravu fungicídov na báze pyritiónu. Cetylpyridínium a laurylpyridínium, ktoré možno vyrobiť z pyridínu Zinckeho reakciou, sa používajú ako antiseptikum v produktoch ústnej a zubnej starostlivosti. Pyridín je ľahko napadnuteľný alkylačnými činidlami za vzniku N-alkylpyridíniových solí. Jedným príkladom je cetylpyridíniumchlorid.  Obr 3-1 Syntéza parakvátu 3.4 Syntéza piperidínu Piperidín, základný dusíkatý heterocyklus, je dôležitým syntetickým stavebným kameňom. Piperidíny sa vyrábajú hydrogenáciou pyridínu s katalyzátorom na báze niklu, kobaltu alebo ruténia pri zvýšených teplotách. C5H5N + 3 H2 -> C5H10NH3,5 Ligand a Lewisova báza Pyridín je široko používaný ako ligand v koordinačnej chémii. Ako ligand kovového komplexu ho možno ľahko nahradiť silnejšou Lewisovou bázou, ktorá sa dá použiť pri katalýze polymerizačných a hydrogenačných reakcií. Po ukončení reakcie môže byť pyridínový ligand nahradený počas reakcie opäť obnovený. Pyridín sa tiež používa ako zásada pri kondenzačných reakciách. Ako zásada sa môže použiť pyridín ako činidlo podľa Karla Fischera, ale zvyčajne sa nahrádza alternatívami s príjemnejšou vôňou, ako je imidazol. 3.6 Iné Okrem vyššie uvedených použití sa pyridín používa aj na výrobu polykarbonátových živíc, vitamínov, potravinárskych aróm, farieb, farbív, gumových výrobkov, lepidiel a hydroizolácií na tkaniny. Pyridín sa pridáva do etanolu, aby bol nevhodný na pitie. Používa sa tiež pri syntéze DNA in vitro. |
| Informácie o toxicite | 4.1 Úroveň toxicity Nízka toxicita 4.2 Akútna toxicita LD501580 mg/kg (veľké myši, orálne); 1121 mg/kg (králik, cez kožu); inhalované človekom 25mg/m3×20 min, podráždenie spojiviek a sliznice horných dýchacích ciest. Subakútna a chronická toxicita: inhalované veľkými myšami 32,3 mg/m3×7 hodín/deň x5 dní/týždeň x6 mesiacov, zvýšenie hmotnosti pečene; vdychované ľuďmi 20-40mg/m3 (dlhodobe), poškodenie nervov, nestabilná chôdza, chvenie prstov, nízky krvný tlak, nadmerné potenie, občasné poškodenie pečene a obličiek. |
| Nebezpečenstvá | 5.1 Zdravotné riziká Pyridín je extrémne toxický pri požití a vdýchnutí. Pary sú ťažšie ako vzduch. jeho spaľovaním vznikajú toxické oxidy dusíka. Pyridín je vysoko horľavý (bod vzplanutia je len 17 ºC). Pyridín môže mať aj neurotoxické a genotoxické účinky. 5.2 Nebezpečenstvo požiaru Správanie sa pri požiari: Výpary sú ťažšie ako vzduch a môžu prejsť značnú vzdialenosť k zdroju vznietenia a vzplanúť. |
| Referencie |
https://en.wikipedia.org/wiki/Pyridine#Occurrence http://www.zwbk.org/MyLemmaShow.aspx?zh=zh-tw&lid=169038 http://www.softschools.com/formulas/chemistry/pyridine{0}}vzorec/378/ http://www.hmdb.ca/metabolites/HMDB0000926 https://study.com/academy/lesson/pyridine-in-medicine-uses-synthesis.html#partialRegFormModal http://www.toxipedia.org/display/toxipedia/Pyridine https://www.chemicalbook.com/ProductChemicalPropertiesCB8852825_SK.htm https://pubchem.ncbi.nlm.nih.gov/compound/pyridine#section=Na začiatok http://www.ebi.ac.uk/chebi/searchId.do;jsessionid=E7088896622D62FC650863C2AD197CAA?chebiId=CHEBI:16227 https://www.britannica.com/science/pyridine Shimizu, S.; Watanabe, N.; Kataoka, T.; Shoji, T.; Abe, N.; Morishita, S.; Ichimura, H. (2005), "Pyridine and Pyridine Derivatives", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a22_399 |
| Chemické vlastnosti | Pyridín je slabo žltá alebo bezfarebná kvapalina; hygroskopické; nepríjemný zápach; horiaca chuť; mierne alkalický v reakcii; rozpustný vo vode, alkohole, éteri, benzéne a mastných olejoch; merná hmotnosť, 0.978; teplota samovznietenia, 482 stupňov. Pyridín, terciárny amín, je o niečo silnejšia zásada ako anilín a ľahko tvorí kvartérne amóniové soli. |
| Chemické vlastnosti | Pyridín je slabá zásada (pKa{{0}}.25); 0,2 M roztok má pH 8,5 (HSDB 1988). Jeho uhlíkové atómy sú deaktivované smerom k elektrofilnej substitúcii. To platí najmä v kyslom prostredí, kde sa na dusíku tvoria soli. Ľahko však podlieha nukleofilnej substitúcii, prednostne v polohe C-2 a tiež v polohe C-4 (Jori et al 1983). Keďže ide o terciárny amín, pyridín reaguje s alkylačnými činidlami za vzniku kvartérnych solí (Santodonato et al 1985). Kvôli svojej zníženej schopnosti darovať elektróny je odolnejší voči oxidácii ako benzén. Oxidáciou s peroxykyselinami vzniká pyridín-N-oxid, ktorý je potom schopný elektrofilnej substitúcie (Jori a kol. 1983). Pyridín prudko reaguje s množstvom zlúčenín, vrátane kyseliny dusičnej, kyseliny sírovej, anhydridu kyseliny maleínovej, perchrómanu, beta-propiolaktónu a kyseliny chlórsulfónovej. Tepelný rozklad môže uvoľniť kyanidy (Gehring 1983). Ako pyridíniový ión, tak samotný pyridín sa ľahko redukujú na komerčne dôležitú zlúčeninu, piperidín (Jori a kol. 1983). |
| Fyzikálne vlastnosti | Číra, bezfarebná až svetložltá, horľavá kvapalina s ostrým, prenikavým zápachom podobným rybám. Prahové koncentrácie zápachu vo vode a vzduchu boli 2 ppm (Buttery et al., 1988) a 21 ppbv(Leonardos a kol., 1969), resp. Detekčné prahové koncentrácie zápachu 0,74 mg/m3(2,3 ppmv) a 6 mg/m3(1,9 ppmv) boli experimentálne stanovené Katzom a Talbertom (1930) a Dravnieksom (1974). Cometto-Mu?iz a Cain (1990) uviedli priemernú prahovú koncentráciu štipľavosti v nose 1 275 ppmv. |
| Výskyt | Pyridín objavil Anderson v uhoľnom dechte v roku 1846 (Windholz a kol. 1983). Nachádza sa v tabakovom dyme (Vohl a Eulenberg 1871; Lehmann 1909) a praženej káve (Bertrand a Weisweiller 1913). Pyridín sa nachádza v drevnom oleji a v listoch a koreňoch Atropa belladonna (HSDB 1988) a je tiež zložkou kreozotového oleja (Krone et al 1986). V prírode sa pyridín a jeho deriváty bežne vyskytujú ako zložky alkaloidov, vitamínov a koenzýmov. |
| Využitie | Pyridín sa používa ako rozpúšťadlo v priemysle farieb a gumy; ako medziprodukt vo farbivách a farmaceutických výrobkoch; na denaturáciu alkoholu a ako činidlo na analýzu kyanidu. Vyskytuje sa v uhoľnom dechte. |
| Využitie | Pyridín sa používa priamo pri denaturácii alkoholu (ACGIH 1986; HSDB 1989; NSC 1978) a ako rozpúšťadlo pri príprave farieb a gumy (ACGIH 1986; HSDB 1989; NSC 1978) a vo výskumných laboratóriách na funkcie, ako je extrakcia rastlinných hormónov ( Santodonato a kol. Polovica dnes vyrábaného pyridínu sa používa ako medziprodukt pri výrobe rôznych insekticídov a herbicídov na poľnohospodárske aplikácie (ACGIH 1986; Harper a kol. 1985; Santodonato a kol. 1985). Približne 20 % ide do výroby piperidínu (Harper a kol. 1985; Santodonato a kol. 1985), ktorý je komerčne významný pri príprave chemikálií používaných pri vulkanizácii gumy a poľnohospodárstve (NSC 1978). Pyridín sa tiež používa ako medziprodukt pri príprave liekov (antihistaminiká, steroidy, sulfátové a iné antibakteriálne činidlá), farbív, vodoodpudivých látok a polykarbonátových živíc (ACGIH 1986; Harper a kol. 1985; NSC 1978; Santodonato a kol. 1985). Pyridín je tiež schválený Food and Drug Administration (FDA) na použitie ako dochucovadlo pri príprave potravín (Harper a kol. 1985; HSDB 1989). |
| Definícia | ChEBI: Pyridín je azaarén obsahujúci benzénové jadro, v ktorom je jedna skupina -CH nahradená atómom dusíka. Je to materská zlúčenina triedy pyridínov. Molekuly majú šesťuholníkový rovinný kruh a sú izoelektronické s benzénom. Pyridín je príkladom aromatickej heterocyklickej zlúčeniny s elektrónmi vo väzbách uhlík-uhlík pi a osamoteným párom dusíka delokalizovaným v kruhu atómov. Zlúčenina sa extrahuje z uhoľného dechtu a používa sa ako rozpúšťadlo a surovina pre organickú syntézu. |
| Výrobné metódy | Pyridín sa vyrába z plynov získaných koksovaním uhlia a priamou syntézou. Ľahká olejová frakcia uhoľného dechtu sa spracuje kyselinou sírovou za vzniku vo vode rozpustných pyridínových solí a potom sa pyridínové bázy získajú z vodnej fázy hydroxidom sodným alebo amoniakom (Jori a kol. 1983). Väčšina americkej produkcie sa vyrába syntetickými prostriedkami. Tento proces využíva reakciu acetaldehydu, formaldehydu a amoniaku v plynnej fáze, ktorá poskytuje zmes pyridínu a 3-metylpyridínu (Santodonato et al 1985). Pomer produktu závisí od relatívnych množstiev acetaldehydu a formaldehydu. Pridaný metanol zvyšuje výťažok. Produkcia pyridínu v USA sa v roku 1975 odhadovala na 32 až 47 miliónov libier (Reinhardt a Brittelli 1981). Pyridín je komerčne dostupný v technických stupňoch 2 a 1 stupňoch, pričom posledné dva sa vzťahujú na ich rozsahy varu. Hlavnými nečistotami sú homológy s vyššou teplotou varu, ako sú pikolíny, lutidíny a kolidíny, čo sú mono-, di- a trimetylpyridíny (Santodonato a kol. 1985; Jori a kol. 1983). |
| Príprava | Pyridín sa vyrába buď izoláciou z prírodných zdrojov, ako je uhlie, alebo chemickou syntézou (HSDB 1989). Pyridín sa vyrába frakčnou destiláciou zvyškov uhoľného dechtu (HSDB 1989; NSC 1978; Santodonato et al. 1985), pri ktorej 1 tona uhlia vyprodukuje 0.07-0,21 libier pyridínových báz z ktorých 57 % je pyridín (Santodonato et al, 1985). Synteticky vyrobený pyridín je v súčasnosti dôležitejším zdrojom pyridínu na komerčné použitie (Santodonato et al. 1985). Malé množstvá pyridínu sa syntetizujú z acetaldehydu, formaldehydu a amoniaku s fluidizovaným oxidom kremičitým a oxidom hlinitým ako katalyzátorom, po čom nasleduje frakcionácia na izoláciu pyridínu (Harper a kol. 1985; HSDB 1989; NSC 1978). Pyridín vyrába z prírodných zdrojov Crowley Tar Products of Stow, Ohio a Oklahoma City, Oklahoma (Harper a kol. 1985; HSDB 1989; SRI 1986, 1987, 1988). Pyridín synteticky vyrábajú dve spoločnosti, Nepera Chemical Co. z Harriman, New York a Reilly Tar and Chemical Corporation z Indianapolis, Indiana (Harper a kol. 1985; SRI 1986, 1987, 1988). |
| Prahové hodnoty arómy | Detekcia: 0.079 až 790 ppb; rozpoznávanie: 7,9 až 40 ppm |
| Všeobecný popis | Číra bezfarebná až svetložltá kvapalina s prenikavým nepríjemným zápachom. Hustota 0,978 g/cm3. Bod vzplanutia 68 stupňov F. Pary sú ťažšie ako vzduch. Toxický pri požití a vdýchnutí. Pri spaľovaní vznikajú toxické oxidy dusíka. |
| Reakcie vzduchu a vody | Veľmi horľavý. Rozpustný vo vode. |
| Profil reaktivity | Azabenzén je zásada. S kyselinami reaguje exotermicky. Pri príprave komplexu azabenzénu s oxidom chrómovým, kyselinou, sa zvýšil podiel oxidu chrómového. Zahrievanie z tejto acidobázickej reakcie viedlo k výbuchu a požiaru [História prípadov MCA 1284 1967]. 0,1% roztok azabenzénu (alebo iného terciárneho amínu) v anhydride kyseliny maleínovej pri 185 stupňoch poskytuje exotermický rozklad s rýchlym vývojom plynu [Chem Eng. Správy 42(8); 41 1964]. Miešanie azabenzénu v rovnakých molárnych častiach s niektorou z nasledujúcich látok v uzavretej nádobe spôsobilo zvýšenie teploty a tlaku: kyselina chlórsulfónová, kyselina dusičná (70 %), oleum, kyselina sírová (96 %) alebo propiolaktón [NFPA 1991]. Kombinácia jódu, azabenzénu, oxidu sírového a formamidu vytvorila po niekoľkých mesiacoch pretlakovanie plynu. Vznikla pomalou tvorbou kyseliny sírovej z vonkajšej vody alebo dehydratáciou formamidu na kyanovodík. Etylénoxid a SO2 môžu prudko reagovať v roztoku azabenzénu s tlakom, ak je etylénoxidu prebytok (Nolan, 1983, Case History 51). |
| Nebezpečenstvo | Horľavé, nebezpečné nebezpečenstvo požiaru, limity výbušnosti vo vzduchu 1,8–12,4 %. Toxický pri požití a vdýchnutí. Dráždi kožu, poškodenie pečene a obličiek. Pochybný karcinogén. |
| Hazard so zdravím | Akútna toxicita pyridínu je nízka. Vdýchnutie spôsobuje podráždenie dýchacieho systému a môže ovplyvniť centrálny nervový systém, čo spôsobuje bolesti hlavy, nevoľnosť, vracanie, závraty a nervozitu. Pyridín dráždi oči a pokožku a ľahko sa vstrebáva, čo vedie k systémovým účinkom. Požitie pyridínu môže viesť k poškodeniu pečene a obličiek. Pyridín spôsobuje čuchovú únavu a jeho zápach neposkytuje dostatočné upozornenie na prítomnosť škodlivých koncentrácií. Nezistilo sa, že by pyridín bol karcinogénny alebo vykazoval reprodukčnú alebo vývojovú toxicitu u ľudí. Chronická expozícia pyridínu môže viesť k poškodeniu pečene, obličiek a centrálneho nervového systému. |
| Hazard so zdravím | Toxické účinky pyridínu zahŕňajú bolesť hlavy, závraty, nervozitu, nevoľnosť, nespavosť, časté močenie a bolesti brucha. Symptómy boli prechodné, u ľudí sa vyskytli pri subakútnej expozícii pyridínovým výparom pri asi 125 ppm počas 4 hodín denne počas 1-2 týždňov (Reinhardt a Brittelli 1981). Cieľovými orgánmi toxicity pyridínu sú centrálny nervový systém, pečeň, obličky, gastrointestinálny trakt a koža. Cesty expozície sú vdýchnutie pár a požitie a absorpcia kvapaliny cez pokožku. Chronické vdychovanie, ktoré môže spôsobiť poškodenie obličiek a pečene a stimulácia kostnej drene na zvýšenie tvorby krvných doštičiek, môže spôsobiť vážne zdravotné riziká. Nízka expozícia 10 ppm môže spôsobiť chronickú otravu na centrálny nervový systém. Požitie kvapaliny môže vyvolať rovnaké príznaky, ako sú uvedené vyššie. Kontakt s pokožkou môže spôsobiť dermatitídu. Para je dráždivá pre oči, nos a pľúca. Kvôli silnému nepríjemnému zápachu vždy existuje dostatočné varovanie pred nadmernou expozíciou. Koncentrácia 10 ppm je pre ľudí nežiaduca. Hodnota LCLO, inhalácia (potkany): 4000 ppm/4 h Hodnota LD50, orálne (myši): 1500 mg/kg. Huh a spolupracovníci (1986) skúmali účinok kyseliny glycyrrhetínovej na toxicitu pyridínu u myší. Predbežná liečba kyselinou glycyrrhetínovou znížila depresiu centrálneho nervového systému a úmrtnosť zvierat vyvolanú pyridínom. Takáto predliečba výrazne znížila aktivitu enzýmu sérová transamináza a zvýšila aktivitu pečeňovej mikrozomálnej anilínhydroxylázy [9012-90-0], enzýmu metabolizujúceho pyridín. |
| Horľavosť a výbušnosť | Pyridín je vysoko horľavá kvapalina (hodnotenie NFPA=3) a jeho výpary sa môžu dostať na značnú vzdialenosť a „spätne vzplanúť“. Pary pyridínu tvoria so vzduchom výbušné zmesi v koncentráciách 1,8 až 12,4 % (obj.). Pri požiaroch pyridínu by sa mal používať oxid uhličitý alebo suché chemické hasiace prístroje. |
| Priemyselné využitie | Pyridín je dobrým rozpúšťadlom pre veľké množstvo zlúčenín, organických aj anorganických (Windholz a kol. 1983). Asi 50 % pyridínu používaného v USA je na výrobu poľnohospodárskych chemikálií, ako sú herbicídy paraquat, diquat a triclopyr a insekticíd chlorpyrifos. Ďalšie použitia sú pri výrobe piperidínu; výroba liečiv, ako sú steroidy, vitamíny a antihistaminiká; a ako rozpúšťadlo. Použitie rozpúšťadiel sa nachádza vo farmaceutickom priemysle a priemysle polykarbonátových živíc. Je obzvlášť užitočný ako rozpúšťadlo v procesoch, kde sa vyvíja HC1 (Santodonato et al 1985). V menšom rozsahu sa pyridín používa na denaturáciu liehu a nemrznúcich zmesí, ako pomocný prostriedok pri farbení textílií a ako ochucovadlo (Jori a kol. 1983; Furia 1968; HSDB 1988). |
| Kontaktovať alergény | Pyridín (nesubstituovaný pyridín) a jeho derivát (substituované pyridíny) sú široko používané v chémii. Pyridín je rozpúšťadlo používané pre mnohé organické zlúčeniny a chemické bezvodé kovové soli. Obsiahnutý v Karl Fischerovom činidle vyvolal kontaktnú dermatitídu u laboratórneho technika. Medzi týmito rôznymi látkami nebola pozorovaná žiadna skrížená citlivosť. |
| Bezpečnostný profil | Jed intraperitoneálnou cestou. Stredne toxický pri požití, kontakte s pokožkou, intravenóznym a subkutánnym spôsobom. Mierne toxický pri vdýchnutí. Silne dráždi pokožku a oči. Boli hlásené údaje o mutácii. Môže spôsobiť depresiu centrálneho nervového systému, gastrointestinálne ťažkosti a poškodenie pečene a obličiek. Horľavá kvapalina a nebezpečenstvo požiaru pri vystavení teplu, plameňu alebo oxidantom. Vážne nebezpečenstvo výbuchu vo forme pár pri vystavení plameňu alebo iskre. Prudko reaguje s kyselinou chlórsulfónovou, oxidom chrómovým, oxidom dusnatým, HNO3, oleom, perchrómanmi, ppropiolaktónom, AgClO4, H2SO4. Žiarivá reakcia s fluórom. Reaguje za vzniku samozápalných alebo výbušných produktov s fluoridom brómovým, trifluórmetyl hypofluoritom. Zmesi s formamidom + jódom + oxidom sírovým predstavujú nebezpečenstvo pri skladovaní, pričom sa uvoľňuje oxid uhličitý a kyselina sírová. Nekompatibilné s oxidačnými materiálmi. Reaguje s anhydridom kyseliny maleínovej (nad 150 stupňov), pričom sa uvoľňuje oxid uhličitý. Na hasenie požiaru použite alkoholovú penu. Pri zahrievaní do rozkladu uvoľňuje vysoko toxické výpary NOx. |
| Potenciálne vystavenie | Pyridín sa používa ako rozpúšťadlo v chemickom priemysle a ako denaturačné činidlo pre etylalkohol; ako medziprodukt pri výrobe pesticídov; vo farmaceutických výrobkoch; pri výrobe farieb, výbušnín, farbív, gumy, vitamínov, sulfátových liečiv; a dezinfekčné prostriedky. |
| Karcinogenita | Pyridín nebol karcinogénny v niekoľkých chronických subkutánnych štúdiách. Potkanom F344 sa podával pyridín perorálne v pitnej vode v dávkach 0, 7, 14 alebo 33 mg/kg počas 2 rokov. Najvyššia dávka spôsobila zníženie telesnej hmotnosti a spotreby vody. Zvýšený renálny tubulárny adenóm alebo karcinóm a tubulárna hyperplázia boli pozorované u mužov pri dávke 33 mg/kg. Zvýšená mononukleárna bunková leukémia sa pozorovala u samíc pri dávkach 14 a 33 mg/kg, čo sa považovalo za nejednoznačné z hľadiska vzťahu k expozícii pyridínu, keďže ide o bežný nález u tohto kmeňa potkanov. Nenádorové zmeny v pečeni súvisiace s koncentráciou sa pozorovali pri dávke 33 mg/kg. Samce potkanov Wistar boli podobne liečené dávkami 0, 8, 17 alebo 36 mg/kg počas 2 rokov. Znížené prežívanie a telesná hmotnosť boli pozorované pri 17 a 36 mg/kg. Zvýšené adenómy testikulárnych buniek boli pozorované pri dávke 36 mg/kg. Neboli hlásené žiadne zmeny v prežití alebo miere novotvarov v iných tkanivách, vrátane obličiek, hoci u niektorých potkanov liečených pyridínom sa pozorovala zvýšená nefropatia a centrilobulárna degenerácia/nekróza pečene. |
| Zdroj | Pyridín sa prirodzene vyskytuje v zemiakoch, anabáze, listoch kurníku, mäte piepornej (0 až 1 ppb), čajových listoch a listoch tabaku (Duke, 1992). Identifikovaná ako jedna zo 140 prchavých zložiek použitých sójových olejov zozbieraných zo spracovateľského závodu, v ktorom sa vyprážali rôzne produkty z hovädzieho, kuracieho a teľacieho mäsa (Takeoka a kol., 1996). |
| Environmentálny osud | Biologické.Heukelekian a Rand (1955) uviedli hodnotu 5-d BSK 1,31 g/g, čo je 58,7 % z hodnoty ThOD 2,23 g/g. A Nocardia sp. izolovaný z pôdy bol schopný transformovať pyridín v prítomnosti semikarbazidu na medziprodukt identifikovaný ako semialdehyd kyseliny jantárovej (Shukla a Kaul, 1986). 1,4-Dihydropyridín, dialdehyd glutarovej, semialdehyd kyseliny glutarovej a kyselina glutarová boli identifikované ako medziprodukty pri degradácii pyridínu kmeňom Nocardia Z1 (Watson a Cain, 1975). Fotolytické.Ožarovanie vodného roztoku pri 50 stupňoch počas 24 hodín viedlo k výťažku 23,06 % oxidu uhličitého (Knoevenagel a Himmelreich, 1976). Chemické/Fyzikálne.Reakcia ozónu v plynnej fáze s pyridínom v syntetickom vzduchu pri 23 stupňoch poskytla nitrovanú soľ so vzorcom: [C6H5NH]+NO3 - (Atkinson a kol., 1987). Ozonizácia pyridínu vo vodných roztokoch pri 25 stupňoch bola študovaná s a bez pridania terc-butylalkoholu (20 mM) ako lapača radikálov. S terc-butylalkoholom sa ozonizáciou pyridínu získal hlavne pyridín-N-oxid (80 % výťažok), ktorý bol veľmi stabilný voči ozónu. Bez terc-butylalkoholu sa heterocyklický kruh rýchlo štiepi za vzniku amoniaku, dusičnanu a amidovej zlúčeniny kyseliny N-formyloxámovej (Andreozzi et al., 1991). |
| Metabolizmus | Pyridín sa absorbuje cez gastrointestinálny trakt, kožu a pľúca a vylučuje sa močom, stolicou, kožou a pľúcami, a to ako metabolity, tak aj ako materská zlúčenina (Jori et al 1983). Príjem tkanivami sa zvyšuje s dávkou a eliminácia je dvojfázovej povahy (Zharikov a Titov 1982; HSDB 1988). Eliminácia je rýchla a zdá sa, že nedochádza k akumulácii tkaniva (Jori a kol. 1983). His (1887) pozorovanie vylučovania Af-metylpyridínu v moči zvieratami, ktorým bol podávaný pyridín, bolo prvým príkladom Af-metylácie. Medzi známe močové metabolity pyridínu u cicavcov teraz patrí pyridín-N-oxid, N-metylpyridín, 4-pyridón, 2-pyridón a 3-hydroxypyridín. Niektoré metabolity ešte stále nie sú identifikované (Damani a kol. 1982). Relatívne množstvá metabolitov sú vysoko závislé od druhu a dávky (Gorrod a Damani 1980). Napríklad sa ukázalo, že potkan vylúči 70 % z dávky 1 mg/kg močom počas prvých 24 hodín po podaní dávky, ale toto číslo klesá len na 5,8 % pri dávke 500 mg/kg (D'Souza et al 1980). Hoci vylučovanie pyridínu a jeho metabolitov močom sa zdá byť hlavnou cestou eliminácie, vylučovanie mimo moču nebolo extenzívne skúmané (Santodonato et al 1985). U králikov sa ukázalo, že aktivita pyridín N-metyltransferázy je najvyššia v pľúcnom cytosóle a zistilo sa, že ako donor metylu využíva 5-adenosylmetionín (Damani et al 1986). Táto dráha je saturovateľná u potkanov aj u morčiat (D'Souza et al 1980). Produkt tejto reakcie, N-metylpyridín, je menej chronicky toxický, ale akútnejší ako pyridín (Williams 1959). Pyridín-N-oxid je produkovaný systémom cytochrómu P-450 a aktivita je vyvolaná predbežnou úpravou fenobarbitalom alebo pyridínom, ale nie {3-metylcholantrénom (Gorrod a Damani 1979; Kaul a Novak 1987). U králika alkoholom indukovateľný (a pyridínom indukovateľný) P-450 LM3AZdá sa, že je nízke Kmizozým, ktorý katalyzuje produkciu pyridínu Af-oxidu (Kim a Novak 1989). N-oxidácia pyridínu môže predstavovať cestu bioaktivácie (Santodonato a kol. 1985) a táto cesta sa stáva dôležitejšou, keď sa zvyšuje dávka pyridínu (Damani a kol. 1982). |
| skladovanie | Pyridín by sa mal používať iba v priestoroch bez zdrojov vznietenia a množstvá väčšie ako 1 liter by sa mali skladovať v tesne uzavretých kovových nádobách v priestoroch oddelených od oxidačných činidiel. |
| Doprava | UN1992 Horľavé kvapaliny, toxické, nie, Trieda nebezpečnosti: 3; Štítky: 3-Horľavá kvapalina, 6.{4}}Jedovaté materiály, vyžaduje sa technický názov. |
| Spôsoby čistenia | Pravdepodobnými nečistotami sú H2O a amíny, ako sú pikolíny a lutidíny. Pyridín je hygroskopický a je miešateľný s H2O a organickými rozpúšťadlami. Môže sa sušiť pevným KOH, NaOH, CaO, BaO alebo sodíkom, po čom nasleduje frakčná destilácia. Ďalšie spôsoby sušenia zahŕňajú státie na molekulárnych sitách Linde typu 4A, CaH2 alebo LiAlH4, azeotropickú destiláciu H2O s toluénom alebo *benzénom alebo spracovanie s fenylmagnéziumbromidom v éteri, po ktorom nasleduje odparenie éteru a destilácia pyridínu. Odporúčaná metóda [Lindauer Mukherjee Pure Appl Chem 27 267 1971] suší pyridín nad pevným KOH (20 g/kg) počas 2 týždňov a frakčne destiluje supernatant cez molekulárne sitá Linde typu 5A a pevný KOH. Produkt sa skladuje pod dusíkom bez CO{10}}. Pyridín sa môže skladovať v kontakte s BaO, CaH2 alebo molekulovými sitami. Nezásadité materiály možno odstrániť destiláciou s vodnou parou roztoku obsahujúceho 1,2 ekvivalentu 20 % H2S04 alebo 17 % HCl, kým sa asi 10 % zásady neprenesie spolu s nezásaditými nečistotami. Zvyšok sa potom zalkalizuje a zásada sa oddelí, vysuší NaOH a frakčne destiluje. Alternatívne môže byť pyridín spracovaný oxidačnými činidlami. Takto sa pyridín (800 ml) miešal 24 hodín so zmesou síranu ceričitého (20 g) a bezvodého K2C03 (15 g), potom sa prefiltroval a frakčne destiloval. Hurd a Simon [J Am Chem Soc 84 4519 1962] miešali pyridín (135 ml), vodu (2,5 1) a KMn04 (90 g) počas 2 hodín pri 100 °C, potom stáli 15 hodín a potom sa odfiltrovali vyzrážané oxidy mangánu. Pridanie pevného KOH (cca 500 g) spôsobilo oddelenie pyridínu. Zmes sa dekantovala, refluxovala s CaO počas 3 hodín a destilovala. Oddelenie pyridínu od niektorých jeho homológov sa môže dosiahnuť kryštalizáciou oxalátov. Pyridín sa vyzráža vo forme oxalátu jeho pridaním k miešanému roztoku kyseliny šťaveľovej v acetóne. Zrazenina sa odfiltruje, premyje studeným acetónom a pyridín sa regeneruje a izoluje. Iné metódy sú založené na tvorbe komplexov so ZnCl2 alebo HgCl2. |
| Nekompatibility | Prudká reakcia so silnými oxidačnými činidlami; silné kyseliny; kyselina chlórsulfónová; anhydrid kyseliny maleínovej; oleum jód. |
| Likvidácia odpadu | Riadené spaľovanie, pri ktorom sa oxidy dusíka odstraňujú z odpadových plynov pomocou práčky, katalytických alebo tepelných zariadení. |
| Produkty a suroviny na prípravu pyridínu |
| Suroviny | Sulfuric acid-->Ammonia-->Benzene-->COAL TAR-->3-Picoline-->COKEOVENGAS-->1,5-DIHYDROCHLORID DIAMINOPENTÁNU |
| Produkty na prípravu | Methyl 2-Fluoroisonicotinate-->2-ACETYL-5-CYANOTHIOPHENE-->5-BROMO-2-FLUOROCINNAMIC ACID-->4-NITROISOPHTHALIC ACID-->3,5-DIMETHOXYCINNAMIC ACID-->2-(2-Butoxyethoxy)ethyl acetate-->2,4-MESITYLENEDISULFONYL DICHLORIDE-->(4-FLUORO-BENZYL)-METHYL-AMINE-->1-Phenacylpyridinium bromide-->3-(TRIFLUOROMETHOXY)CINNAMIC ACID-->trans-Ferulic acid-->3-(Trifluoromethyl)pyrazole-->4-Fluorocinnamic acid-->Indigosol Green Blue IBC-->2-Amino-4-methyl-5-acetylthiazole-->Benzyl 2-chloroacetate-->5-ACETAMIDONICOTINIC ACID-->7-ACETOXYCOUMARIN-->2-AMINO-4-METHYL-QUINOLINE-3-CARBONITRILE-->N-PHENYLISONICOTINAMIDE-->Allyl methyl carbonate-->Pyridine-3-sulfonyl chloride hydrochloride-->Syringaldehyde-->2,4,5,6-TETRAMETHYLBENZENEDISULFONYL DICHLORIDE-->3-(3-METHYL-2-THIENYL)ACRYLIC ACID-->Vat Grey M-->17beta-Hydroxy-17-methylandrosta-4,9(11)-dien-3-one-->butyl N-phenylcarbamate-->3-Methoxycinnamic acid-->1-CHLORO-2-METHYLPROPYL CHLOROFORMATE-->Pyrazinecarbonitrile-->2-AMINO-6-CHLORO-3,5-DICYANOPYRIDINE-->4-BROMO-TETRAHYDROPYRAN-->Phenylcarbamic acid propyl ester-->Hydrocortisone acetate-->5-METHYLPICOLINIC ACID-->4-Acetamido-2-chloropyridine-->Pyridinium p-Toluenesulfonate-->1,2,4-Triazolo[4,3-a]pyridin-3(2H)-one-->Paraquat dichlorid |
Populárne Tagy: pyridín, Čína výrobcovia pyridínu, dodávatelia, továreň
Tiež sa vám môže páčiť
Zaslať požiadavku







