| Chemické vlastnosti |
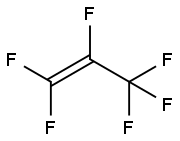
Hexafluórpropylén (HFP) je bezfarebný nehorľavý plyn bez zápachu, ktorý je len málo rozpustný vo vode. Používa sa ako chemický medziprodukt predovšetkým pri syntéze fluórpolymérov, fluórelastomérov a fluórovaných materiálov (napr. perfluórpolyéterové funkčné kvapaliny, oleje a tuky). |
| Využitie |
Hexafluórpropén sa používa pri syntéze polyvinylidénfluorid-ko-hexafluórpropylénu, polyméru, ktorý sa v súčasnosti používa v rôznych oblastiach nano a elektronického sektora, od membrán až po nanočastice. |
| Príprava |
Hexafluórpropylén možno vyrobiť pyrolýzou tetrafluóretylénu (TFE):
3 CF2=CF2 → 2 CF3CF=CF
Táto reakcia sa uskutočňuje v uzavretom kontinuálnom reaktore pri teplote 600 až 900 stupňov. Výťažok možno zlepšiť pri nízkom parciálnom tlaku, ktorý sa dosiahne buď prevádzkou pri zníženom celkovom tlaku (až na 0,1 baru) alebo vstrekovaním inertného riedidla, ako je para alebo CO2.
Počas pyrolýzy TFE vzniká značné množstvo vedľajších produktov, vrátane vysoko toxického perfluórizobutylénu (PFIB). Takéto vedľajšie produkty sa buď priamo spaľujú, alebo sa zbierajú a prepravujú na spálenie vo vzdialenom zariadení.
Hexafluórpropylén možno tiež pripraviť z chlórdifluórmetánu alebo vyrobiť z rôznych chlórfluórovaných uhľovodíkov. |
| Syntéza referencie |
Journal of the American Chemical Society, 73, s. 4054, 1951DOI:10.1021/ja01152a548 |
| Všeobecný popis |
Hexafluórpropylén je bezfarebný plyn bez zápachu. Hexafluórpropylén je nehorľavý. Hexafluórpropylén sa môže zadusiť vytlačením vzduchu. Vystavenie nádoby dlhodobému teplu alebo ohňu môže spôsobiť prudké roztrhnutie hexafluórpropylénu a výbuch. |
| Profil reaktivity |
Halogénované alifatické zlúčeniny, ako je hexafluórpropylén, sú stredne alebo veľmi reaktívne. Reaktivita všeobecne klesá so zvýšeným stupňom substitúcie atómov vodíka halogénom. Materiály v tejto skupine môžu byť nekompatibilné so silnými oxidačnými a redukčnými činidlami. Tiež môžu byť nekompatibilné s mnohými amínmi, nitridmi, azo/diazo zlúčeninami, alkalickými kovmi a epoxidmi. Nad minimálnym tlakom kyslíka sa reakcia difluoridu kyslíka a hexafluórpropénu za vzniku hexafluórpropylénoxidu stáva výbušnou, Chem. Abs., 1987, 107, 175302. Reakcia hexafluórpropénu s Grignardovým činidlom (subst. fenylmagnéziumbromidy) viedla k výbuchu, Fluorine Chem., 1981, 18, 25. |
| Zdravotné nebezpečenstvo |
Výpary môžu bez varovania spôsobiť závraty alebo zadusenie. Pary zo skvapalneného plynu sú spočiatku ťažšie ako vzduch a šíria sa pri zemi. Kontakt s plynom alebo skvapalneným plynom môže spôsobiť popáleniny, vážne poranenia a/alebo omrzliny. Oheň môže vytvárať dráždivé, korozívne a/alebo toxické plyny. |
| Nebezpečenstvo požiaru |
Niektoré môžu horieť, ale žiadne sa ľahko nevznietia. Nádoby môžu pri zahrievaní explodovať. Prasknuté valce môžu vybuchnúť. |
| Horľavosť a výbušnosť |
Nehorľavý |